بهبود عملکرد عضلات با ژن درمانی دیستروفی عضلانی دوشن
طبق مطالعه ای از محققان پزشکی Penn Medicine ، یک ژن درمانی در Penn Medicine برای درمان دیستروفی عضلانی دوشن (DMD) ایجاد شده است که با موفقیت و ایمنی از وخامت شدید عضلات مرتبط با این بیماری نادر ژنتیکی در هر دو مدل حیوانی کوچک و بزرگ جلوگیری میکند. این یافته ها ، که امروز به طور آنلاین در Nature Medicineمنتشر شده است ، زمینه را برای دسترسی به ژن درمانی ایمن و مؤثر که از پروتئین "جایگزین" استفاده می کند ، بدون ایجاد پاسخ های ایمنی شناخته شده در سایر روشهای درمانی ، فراهم میکند.
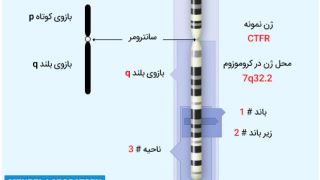
DMD که بیشتر در پسران یافت میشود ، ناشی از جهشهایی در ژن وابسته به جنس است که تولید پروتئین سازنده عضله معروف به دیستروفین را متوقف می کنند. بدون وجود این پروتئین ، ماهیچه ها در سنین نوجوانی به تدریج ضعیف شده و رو به زوال میروند. بیشتر بیماران در سن 12 سالگی قادر به راه رفتن نیستند و زمانی که به 30 سالگی میرسند در اثر نارسایی قلبی یا تنفسی جان خود را از دست می دهند ، اگرچه دستگاه های تنفس مصنوعی به بعضی از افراد کمک میکنند بیشتر عمر کنند.
تیمی چند رشته ای از دانشکده پزشکی پرلمن در دانشگاه پنسیلوانیا با روش ژن درمانی اصلاح شده خود ، وکتور های ویروسی مرتبط با ویروس آدنو(AAV ) را مهندسی کردند تا یک پروتئین "جایگزین" برای دیستروفین را در مدل های DMD حیوانات کوچک و بزرگ برای حفظ ماهیچه ها ارائه دهند. جایگزین مصنوعی بر اساس یک پروتئین طبیعی به نام یوتروپین ، یک جایگزین مؤثر و ایمن ، میباشد زیرا عضلات را در موش ها و سگ هایی که دارای جهش های طبیعی ایجاد شده مانند جهش های DMD هستند و شامل یک حذف بزرگ میباشند که بسیار به جهش های بزرگ دیستروفین انسان شبیه است ، حفظ میکند.
دکتر Hansell H. Stedman ، نویسنده ارشد این مطالعه و استادیار جراحی گفت : " برای اولین بار ما نشان داده ایم كه چگونه یك نسخه با دقت ساخته شده از پروتئین مرتبط با دیستروفین می تواند بطور ایمن از تجزیه ماهیچه ها جلوگیری كرده و عملکرد خود را با گذشت زمان در مدل های حیوانی حفظ كند. این كشف پیامدهای مهمی برای ژن درمانی و چگونگی تلاش ما به سمت درمان های ایمن و مؤثر برای دیستروفی عضلانی داشته است. " "با این نتایج ، ما یک دلیل منطقی داریم که بتوانیم این کار را به سمت کارآزمایی بالینی انسانی سوق دهیم."
با توجه به واکنش شدید سیستم ایمنی بدن به افزودنیهای خارجی ، سطح بازیابی شده دیستروفین از طریق ژن درمانی و سایر روشها مورد بررسی قرار گرفت. بیماران مبتلا به DMD هیچ یک از این پروتئین ها را ندارند ، بنابراین بدن آنها می تواند به پروتئین های جایگزین بطور مستقیم و هدفمند حمله کند زیرا این پروتئین ها به عنوان عوامل خارجی دیده می شوند. با این حال ، از آنجا که یوتروپین ، پسرعموی دیستروفین ، در سایر نقاط بدن بیان شده است ، تصور می شد که سیستم ایمنی آن را به عنوان یک تهدید تلقی نکند.
تیم Penn نشان داد که این نتایج در مطالعات دقیق و تصادفی موشها و سگها صدق میکنند. ارائه یک درمان تک دوزه از یوتروپین مصنوعی با وکتور AAV به موشهای تازه متولد شده نشاندهنده توزیع پروتئین در سراسر بدن ، بدون علامتی از مسمومیت و سرکوب کامل تمام علائم DMD در مقایسه با موشهایی بود که درمان نشده اند. همچنین در طی این مدت بیان یوتروپین در عضلات اسکلتی و قلبی در موش ها پایدار بود و آزمایشهای فیزیکی در موشها عملکرد پایدار ماهیچه ها را نشان میدادند.
این تیم بعلاوه در یک مطالعه تصادفی یوتروپین را با بکارگیری آن در سگهای چهار تا هفت روزه مورد بررسی قرار داد. شش هفته پس از دریافت دوز ، محققان بیان قدرتمند یوتروپین و افزایش چهار برابری وزن نسبت به کاهش وزن و التهاب سراسر بدن که قبلاً گزارش شده بود را مشاهده کردند که این امر نشاندهنده القای سیستم ایمنی خودکار در سگهایی بود که دیستروفین انسانی را دریافت کرده بودند. گروه Penn همچنین میزان قابل توجهی از کاهش آسیب عضلات را در سگهای تحت درمان مشاهده کردند.
در شاید مهمترین مطالعه بر روی سگ ها ، محققان اندامهای تحت درمان با یوتروپین را با اندامهای تحت درمان با دیستروفین مقایسه کردند و پس از چهار هفته اختلافات آشکاری را مشاهده کردند. بیوپسی های عضلانی بیان مداوم یوتروپین و سرکوب آسیب های مداوم عضلات را نشان دادند ، اما تنها مقادیر کمی از دیستروفین در سلول های در حال مرگ در اندامهای دیگر وجود داشتند. پاسخ ایمنی نیز بین اندام ها متفاوت بود.
استدمن گفت : "در زیر میکروسکوپ به نظر می رسید که یک نارنجک دستی در اندام های دارای دیستروفین خاموش شده است." "آزمایشات نشان دادند که پاسخ ایمنی به دیستروفین 100 تا 1000 برابر قویتر از پاسخ ایمنی نسبت به یوتروپین بود."
بعلاوه در سگهای درمان شده به طور نسبتا کامل از تخریب و احیا عضلات نزدیک به فك (عضلات مربوط بهگاز گرفتن) جلوگیری شده بود. این عضلات به واسطه قدرت شدیدشان جزء اولین عضلاتی هستند که در سگهای دیستروفیک درمان نشده رو به زوال میروند.
این اولین مطالعه بزرگ بر روی حیوانات است که اثربخشی یوتروپین و همچنین پاسخ غیرایمونوژنیک آن را نشان می دهد. محققان گفتند ، این یافته ها مجموعا می توانند مجددا زمینه را برای استفاده از یک روش ژن درمانی بهینه و ایمن مبتنی بر یوتروپین که به عنوان یک مسیر درمانی بالقوه دیستروفی عضلانی دوشن میباشد فراهم کنند.
برای ایجاد نسخه مصنوعی Penn ، تیمی از محققان ابتدا به زیست شناسی تکاملی روی آوردند تا بتوانند منشأ دیستروفین و نحوه گردآوری (مونتاژ) آن را بهتر بشناسند و به عقب برگردند و حوادث ژنتیکی را در اولین بخش های تاریخ زمین بازسازی کنند. مطالعات مداوم اطلاعات بیشتری را در مورد آرایش پروتئین ، استحکام ساختار میله ای آن و حذف آن درمیان ویژگی های مهم دیگر برای آگاهی از توسعه آینده نشان می دهند.
استدمن گفت : " ما اطلاعات زیادی را از این رویکرد کسب کرده ایم." "یکی از کارهایی که امیدواریم در طول توسعه بالینی انجام دهیم ، استفاده از این بینش برای ایجاد روشهای درمانی بهتر ، قویترین نسخه های ممکن " نانوتروپین "است."