از آنتی بادی های خنثی کننده برای درمان COVID-19 چه می دانید؟
داده های کارآزمایی بالینی بیشتری برای تعیین اینکه آیا سرم بیماران مبتلا به COVID-19 و خنثی سازی آنتی بادی های مونوکلونال خاص آنتی ژن های SARS-CoV-2 می تواند از COVID-19 جلوگیری کند یا شدت بیماری را در جمعیت های پرخطر کاهش دهد ، مورد نیاز است.
در طول عفونت های ویروسی ، سیستم ایمنی بدن دو نوع آنتی بادی ایجاد می کند. آنها آنتی بادی ها (NAbs) و آنتی بادی های خنثی کننده (n-NAbs) را خنثی می کنند. n-NAbs فعالیت ضد ویروسی را در برابر مناطق محافظت شده از گلیکوپروتئین پاکت (Env) نشان می دهد. NAbs بخش مهمی از پاسخ ایمنی بدن انسان است که شامل یک رابطه پیچیده بین سیستم ایمنی ذاتی و سازگار برای جلوگیری از عفونت است. شناسایی NAbs مشخصه عفونت ویروسی در بیماران مبتلا به آنفلوانزا ، هپاتیت ، HIV ، دانگ و ویروس ابولا است.
همه این ویروس ها با تنوع ژنتیکی بالا در اپیتوپ های پوششی ویروسی مشخص می شوند که به دلیل سرعت تکثیر بالا توسط ماشین های تکثیر مستعد خطا بوجود می آیند. در مقابل ، تنها 10 تا 30 درصد از افراد آلوده آنتی بادی های خنثی کننده وسیع (bNAbs) ایجاد می کنند که فعالیت خنثی سازی گسترده ای را نشان می دهند ، و این bNAbs بعد از 2-4 سال عفونت یافت می شود. اپی توپ های ویروسی Env که سایت ها را مورد هدف قرار می دهند و تکامل bNAbs اطلاعات ارزشمندی را برای طراحی واکسن ارائه می دهند. بنابراین ، شناسایی آنتی بادی های خنثی کننده وسیع راه هایی را برای استفاده از آنها به عنوان ابزار درمانی و همچنین ارائه اطلاعات ارزشمند در مورد اپی توپ های محافظت شده به عنوان اهداف احتمالی واکسن باز کرده است.
آنتی بادی های خنثی کننده (nAbs) می توانند قبل یا بعد از عفونت ویروسی برای پیشگیری یا درمان بیماری به صورت غیرفعال به افراد منتقل شوند (از طرف دیگر واکسن ها به طور فعال سیستم ایمنی را برای تولید nA های اختصاصی آنتی ژن برای جلوگیری از بیماری تحریک می کنند). nAbs درمانی به طور کلی برای مدت کوتاهی در بدن وجود دارد و اثر درمانی آنها بستگی به عوامل مختلفی از جمله تیتر nAb ، مقدار کل ، ویژگی و نیمه عمر دارد. برای درمان عفونت های ویروسی ناشی از ویروس ابولا ، سیتومگالوویروس ، ویروس آنفلوانزا ، ویروس نقص ایمنی بدن انسان و ویروس سینسیتیال تنفسی از آنتی بادی های خنثی کننده با ویژگی بالا ، میل شدید به پروتئین های هدف و سمیت کم استفاده شده است. در این نظر ، ما آنتی بادی های خنثی کننده ، از جمله آنتی بادی های مونوکلونال (mAbs) و نانوبیسم ها را برای سندرم حاد تنفسی شدید کرونا ویروس 2 (SARS-CoV-2) که در حال حاضر در مراحل توسعه پیش بالینی و در آزمایشات بالینی هستند ، به طور خلاصه ، مکانیسم های بالقوه آنتی بادی ها را خلاصه می کنیم. اقدامات ، و کاربردهای بالینی احتمالی mAbs و سرم های دوره نقاهت از بیماران بهبود یافته از عفونت SARS-CoV-2 برای پیشگیری و درمان بیماری کرونا ویروس 2019 (COVID-19).
برخلاف SARS-CoV ، که اولین بار در سال 2003 گزارش شد و با انتقال مشروط به انسان 1 مشخص شد ، SARS-CoV-2 به طور تصاعدی گسترش یافته و منجر به مرگ بیش از 1.3 میلیون نفر در اثر COVID-19 یازده ماه پس از شناسایی شده است. به SARS-CoV-2 و SARS-CoV ، که متعلق به نسل بتا-CoV Coronaviridae هستند ، گیرنده یکسانی دارند-آنزیم تبدیل کننده آنژیوتانسین 2 (ACE2)-برای ورود ویروس به سلولهای میزبان از طریق پروتئین های اسپایک (S) در سطح ویروس 2 برای هر دو ویروس ، پروتئین S از زیرواحد S1 و S2 تشکیل شده است. دامنه اتصال گیرنده (RBD) در زیر واحد S1 ابتدا گیرنده ACE2 را روی سلول ها متصل می کند تا از طریق تشکیل کمپلکس RBD-ACE2 واسطه ورود ویروس شود.
سپس پروتئین S تحت تغییر شکل قرار می گیرد و منجر به همجوشی غشاء و واسطه زیر واحد S2 می شود. پروتئین S یک هموترایمر تشکیل می دهد و می تواند با یک یا چند RBD دچار تغییر شکل خود به خود شود و از حالت "دراز کشیدن" به حالت ایستاده تغییر وضعیت دهد تا اتصال گیرنده ها امکان پذیر شود. پروتئین های ساختاری SARS-CoV-2-یعنی S ، نوکلئوکپسید (N) ، غشای (M) و پاکت (E)-نقش مهمی در عفونت و تکثیر ویروسی ایفا می کنند. درک ساختار و عملکرد این پروتئین ها ، به ویژه پروتئین S و RBD آن زمینه ای برای طراحی و توسعه منطقی nAbs مخصوص SARS-CoV-2 برای پیشگیری و درمان COVID-19 فراهم می کند.
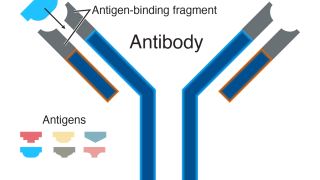
تفاوت قابل ملاحظه ای بین mAbs خنثی کننده و نانو بدن وجود دارد. آنتی بادی های مونوکلونال و قطعات آنها به طور معمول بزرگ هستند و برای حفظ ساختار و عملکرد آنها ، اکثر آنها باید در سیستم های بیان سلول های پستانداران (مانند خطوط سلولی پایدار) تولید شوند ، که معمولاً دارای عملکرد بیان نسبتاً کم و در نتیجه هزینه های تولید بالا هستند. در مقابل، نانو بادی ها آنتی بادی های یک دامنه با اندازه کوچک، حلالیت خوب و پایداری قوی در برابر شرایط شدید هستند. آنها می توانند به راحتی در اشرشیاکلی و سلولهای مخمر در مقیاس بزرگ تولید شوند که منجر به عملکرد بالای بیان، عملکرد خوب و کاهش قابل توجه هزینه های تولید می شود. به دلیل اندازه کوچک آنها، نانوبیسمها معمولاً ترخیص کالا از گمرک کلیه بیشتر و در نتیجه نیمه عمر کوتاه تری نسبت به mAbs دارند. با این حال، نیمه عمر نانو بدن ها را می توان با ترکیب پروتئین های طولانی مدت مانند آلبومین یا ناحیه متبلور (Fc) انسان افزایش داد.
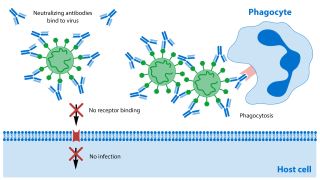
در غیاب آنتی بادی های خاص ، SARS-CoV-2 گیرنده ACE2 را از طریق RBD در زیر واحد S1 متصل می کند ، واسطه ورود ویروس و همجوشی غشای بعدی است. در صورت هدف قرار دادن nAbs و اتصال به RBD SARS-CoV-2 (یا SARS-CoV) ، تعامل با گیرنده ACE2 مسدود شده و همجوشی غشا مهار می شود.
با این حال، چندین nAbs با هدف RBD-یا nAbs با هدف RBD که با گیرنده ACE2 رقابت نمی کنند-اپی توپ های متمایز از موتیف اتصال دهنده ACE2 یا مناطق غیر RBD پروتئین S را تشخیص می دهند. این آنتی بادی ها دارای خاصیت خنثی کننده ویروس هستند. آنها ممکن است NTD را در زیر واحد S1 یا S trimer متصل کنند تا از تغییر شکل پروتئین S جلوگیری کند ، یا ممکن است S2 را برای مهار همجوشی غشاء و ورود ویروس متعاقب آن متصل کنند. در موارد دیگر ، nAbs ممکن است به سلولهای حاوی گیرنده Fcγ (FcγR) متصل شده و منجر به سمیت سلولی وابسته به آنتی بادی (با واسطه سلولهای کشنده طبیعی) یا فاگوسیتوز سلولی وابسته به آنتی بادی شود.
کاربردهای بالینی بالقوه
پلاسمای بیمار در حال بهبودی با فعالیت خنثی کننده قوی و بدون اجزای مضر در نهایت ممکن است برای درمان بیماران مبتلا به COVID-19 مفید باشد. ارتباط تیترهای nAb با تیتر آنتی بادی های اختصاصی RBD یا S1 خاص به منظور شناسایی پلاسما با آنتی بادی های خنثی کننده بسیار موثر و ایمن بسیار مهم خواهد بود. همچنین ، بیماران مبتلا به بیماریهای همراه و پلاسمای دوران نقاهت که ممکن است منجر به ADE52 شود باید برای انتقال پلاسما حذف شوند تا خطر عوارض جانبی احتمالی کاهش یابد. اگرچه سازمان غذا و داروی ایالات متحده مجوز استفاده اضطراری برای استفاده از پلاسمای دوره نقاهت را برای درمان بیماران بستری مبتلا به COVID-19 صادر کرده است ، اما آزمایشات بالینی تصادفی تری برای تعیین اثربخشی و ایمنی پلاسمای دوره نقاهت مورد نیاز است.
استفاده از nAbs مورد آزمایش بالینی برای بیماران مبتلا به COVID-19 نیاز به مطالعه و آزمایش فشرده دارد. با این حال ، همه nAbs اختصاصی SARS-CoV-2 برای حفاظت در برابر عفونت SARS-CoV-2 در مدلهای چالش بر روی حیوانات مورد ارزیابی قرار نگرفته اند و تنها تعداد کمی از آنها در آزمایشات بالینی هستند. داده های کارآزمایی بالینی بیشتری مورد نیاز است. امید این است که کوکتل های آنتی بادی بر اساس nAbs مخصوص اپی توپ های خنثی کننده مختلف در SARS-CoV-2 RBD یا سایر مناطق موجود در پروتئین S SARS-CoV-2 ، درمانهای م effectiveثر COVID-19 را انجام دهند و محافظت کوتاه مدت ایجاد کنند. در برابر عفونت ویروسی در این صورت ، ترکیب تجویز اولیه nAbs به دنبال استروئیدهایی مانند دگزامتازون در مراحل بعدی بیماری (برای کاهش خطر و شدت سندرم پریشانی حاد تنفسی) ممکن است از بارهای زیاد ویروسی و ذات الریه شدید جلوگیری کند و در نتیجه جان افراد را نجات دهد. بر خلاف واکسن ها ، که معمولاً چندین هفته طول می کشد تا تولید آنتی بادی در افراد واکسینه شود 54 ، خنثی سازی mAbs ممکن است محافظت فوری در برابر عفونت ویروسی ایجاد کند و بنابراین برای افراد در تمام سنین مناسب است و به ویژه برای افراد در معرض خطر و افراد دارای نقص ایمنی که معمولاً این کار را می کنند مناسب است. بعد از واکسیناسیون nAbs کافی تولید نکند. با این حال ، تولید mAbs خنثی کننده موثر به شیوه مقرون به صرفه و در مقیاس ، چالش برانگیز است. اکثر mAbs در سلولهای پستانداران با بهره وری نسبتاً پایین و در نتیجه هزینه تولید بالا تولید می شوند. رویکردهای تولیدی که nAbs موثر یا نانودارهای با بازده بالا و هزینه کم تولید کنند ، بسیار مورد نیاز است.
برای ثبت درخواست آزمایش در منزل و یا محل کارتان بر روی لینک زیر کلیک کنید