دیستروفی عضلانی دوشن (و نوع خفیف تر آن دیستروفی عضلانی بکر) ناشی از جهش در ژن DMD می باشند. این بیماری شایع ترین دلیل اختلالات حرکتی در بین جوامع انسانی می باشد. راه های مختلفی برای بررسی انواع موتاسیون های موجود در این بیماری وجود دارد که در ادامه به آنها پرداخته شده است. همچنین شما می توانید از طریق خدمات موجود در سمت چپ این صفحه نوع دقیق تست مورد نیاز را انتخاب نموده و یا برای راهنمایی با کارشناسان ما تماس بگیرید.
بررسی 51 ژن مرتبط با دیستروفی عضلانی به همراه MLPA برای دیستروفی دوشن
بررسی 551 ژن مرتبط با نوروژنتیک و بیماری های عضلانی
بررسی کلیه 23000 ژن (اگزوم) در یک نفر به تنهایی
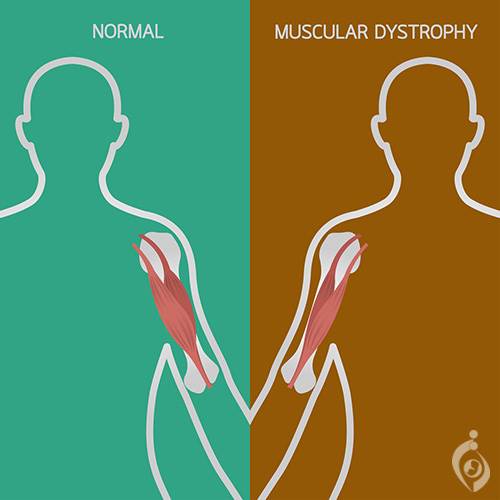
دیستروفی ماهیچه ای دوشن یا Duchenne Muscular Dystrophy (به اختصار DMD) ، شایعترین و شدیدترین نوع از بیماریهای دیستروفی ماهیچهای با الگوی ژنتیکی توارث وابسته به جنس یا وابسته به X است. از عوارض اصلی این بیماری تحلیل و نابودی ماهیچههای ارادی (که در کنترل بدن نقش حیاتی دارند) است که در مواقع شدید نهایتاً منجر به عدم توانایی در راه رفتن ،۹۶% معلولیت، مشکلات تنفسی و مرگ می شود.
فراوانی دوشن ۱ در ۳۵۰۰ کودک پسر است. این بیماری در اثر تغییرات و نقص در ژن (DMD) که بر روی کروموزوم X قرار گرفته است ایجاد میشود. این ژن مسؤل ساخت پروتئین دیستروفین بوده که مادهای ضروری برای حفظ و ثبات ماهیچهها است و در غشاء سلولی قرار دارد. به طور کلی بانوان دارای کروموزوم X ناقص و حامل این بیماری هستند و میتوانند این بیماری را به نیمی از فرزندان پسر خود منتقل کنند. ناقص بودن یکی از کروموزوم های X در بانوان غالباً ارثی است یا ممکن است در اثر جهشهای ژنتیکی باشد (شکل شماره 1 و 2). به طور کلی علایم بیماری در ۶ سالگی ظاهر میشود گرچه در دوران نوزادی هم نمایان است.
نوزاد در موقع تولد کاملاً سالم به نظر میرسد، ولی هنگامی که شروع به حرکت میکند، حتی زمانی که با چهار دست و پا و یا سینه خیز مینماید حرکت او کندتر از همسالان خود است و زود به زود خسته میشود. هنگامی که به راه میافتد ضعف ماهیچه ای به تدریج واضح تر میشود. معمولاً والدین نسبت به نحوه راه رفتن غیر طبیعی یا اشکال در برخاستن فرزندشان از روی زمین، راحت زمین خوردن، اشکال در بالا رفتن از پلهها و عدم توانایی دویدن یا انجام حرکات ورزشی در مقایسه با همسالانشان نگران میشوند.در این بیماری بزرگ شدن غیر طبیعی ماهیچههای ساق پا و ضعف خفیف تا متوسط ماهیچههای ابتدای اندام تحتانی، به صورت راه رفتن اردک وار و عدم توانایی در برخاستن راحت از روی زمین از جمله علائم اصلی به شمار می روند. این کودکان به طور مشخص برای برخاستن از حالت نشسته از پاها و بدنشان کمک میگیرند که به نشانه گاور معروف است (شکل شماره 3). تحلیل ماهیچه ای به صورتی است که در ۸ سالگی کاملاً ضعف ماهیچهها بارز میشود. این تحلیل ماهیچهای ابتدا از پاها و لگن شروع، باعث کاهش حجم و نابودی ماهیچههای این ناحیه میشود و نهایتاً دستها، بازوها و شانه را نیز در بر میگیرد که موجب افتادگی شانه میشود. در ۱۰ سالگی بیمار توانایی راه رفتن را از دست میدهد و به ویلچر نیاز پیدا میکند.
از آنجایی که دو سوم از وزن بدن از ماهیچهها تشکیل شده است، با نابودی ماهیچهها وزن بدن به شدت کاهش می یابد و به یک سوم از کل آن می رسد. در بیشتر مواقع پیشرفت بیماری ادامه مییابد و به علت رشد غیر طبیعی استخوانهای ستون فقرات، ستون فقرات به صورت حرف S انحنا پیدا میکند و قفسه سینه اندکی تغییر شکل می دهد که سبب جمع شدگی بدن می شود. پیشرفت بیماری در مواقع شدید نهایتاً با مشکلات تنفسی و مرگ همراه خواهد بود، طول عمر متوسط برای بیماران معمولاً بین ۲۰ تا ۳۰ سال است.
تصویر شماره 1 – نحوه توارث دیستروفی دوشن
شیوع بیماری دوشن ۱ در ۳۵۰۰ کودک پسر است. به این دلیل این بیماری فقط در جنس مذکر بروز میکند که جنس مذکر فقط یک کروموزوم X دارد . جنس مؤنث به این بیماری مبتلا نمیشود زیرا که در بدن آنها دو کروموزوم X وجود دارد و دوشن فقط در اثر اختلال یکی از کروموزومهای X ایجاد میشود بنابراین آن یکی کروموزوم سالم می ماند و نهایتاً فقط پسران به این بیماری مبتلا میشوند.
نام بیماری دیستروفی ماهیچه ای دوشن برگرفته از نام یک پزشک مختصص مغز و اعصاب فرانسوی به نام گیوم بنیامین اماند دوشن است که اولین بار در سال ۱۸۶۱ شرح بیماری دوشن را در مجلات پزشکی آن زمان منتشر کرد.
بیماری دیستروفی ماهیچه ای دوشن در اثر نقض در کروموزوم X و فقدان پروتئین دیستروفین ایجاد میشود. ژن مسئول ساخت این پروتئین DMD است و بر روی کروموزوم X قرار دارد. پروتئین دیستروفین اطراف سلولهای ماهیچهای برای محافظت ساختمان ماهیچه ساخته میشوند و مانع از خروج عناصر داخل سلول ماهیچه ای به فضای خارج از سلول میشود.بدون دیستروفین سلول ماهیچه ای قابل نفوذ خواهد بود و مواد بافت خارج سلولی وارد سلول ماهیچه شده و باعث تخریب و مرگ ماهیچه خواهد شد و در نهایت بافت چربی جای ماهچه را میگیرد. علت عدم تولید پروتئین دیستروفین در ژن DMD هنوز به طور قطع مشخص نیست ولی این عدم تولید ناشی از مسدود شدن مجاری تولید پروتئین دیستروفین میباشد. پروتئین دیستروفین در بدن افراد طبیعی کمتر از ۰.۰۰۲% میلی گرم از کل پروتئین بافت ماهیچه ای است.
جهش های ژن DMD باعث ایجاد فرم های دوشن و بکر دیستروفی عضلانی میشوند. ژن DMD دستورالعمل هایی برای ساخت پروتئینی به نام دیستروفین فراهم میکند. این پروتئین ابتدا در عضلات اسکلتی و قلبی قرار میگیرد و به پایداری و حفظ رشته های عضلانی کمک میکند. دیستروفین ممکن است در سیگنالینگ شیمیایی درون سلول ها نیز نقش ایفا کند. جهش های ژن DMD ساختار یا عملکرد دیستروفین را تغییر میدهند یا از تولید هرگونه دیستروفین عملکردی جلوگیری میکنند. سلول های عضلانی بدون مقدار کافی از این پروتئین آسیب دیده و عضلات در صورت استفاده ، مکررا انقباض یافته و آزاد میشوند. رشته های آسیب دیده با گذر زمان ضعیف شده و میمیرند که این امر منجر به ضعف عضلانی و مشکلات قلبی ویژه دیستروفی های عضلانی دوشن و بکر میشود. جهش هایی که منجر به ایجاد نوع غیرطبیعی دیستروفین که مقداری از عملکرد خود را حفظ میکند میشوند معمولا باعث ایجاد دیستروفی عضلانی بکر میشوند ، درحالیکه جهش هایی که از تولید هرگونه دیستروفین عملکردی ممانعت میکنند باعث ایجاد دیستروفی عضلانی دوشن میشوند. از آنجائیکه دیستروفی های عضلانی دوشن و بکر از وجود دیستروفین معیوب یا عدم وجود دیستروفین نشات میگیرند ، این بیماری ها به عنوان دیستروفینوپاتی ها طبقه بندی میشوند.
شکل شماره 2- مانور گاور و نحوه برخاستن افراد مبتلا به دیستروفی دوشن
مهمترین نشانه بیماری دیستروفی ماهیچه ای دوشن اختلال در ماهیچه هاست که موجب مشکل در راه رفتن، ضعف ماهیچههای اندام تحتانی و لگن و بزرگ شدن غیر طبیعی ماهیچههای ساق پا میشود. همچنین ضعف ماهیچه ای در دستها، بازو و شانه نیز بروز میکند. نشانهها معمولاً تا قبل از ۶ سالگی ظاهر میشود، هرچند در دوران نوزادی هم نمایان است. نهایتاً پیشرفت این بیماری که موجب نابودی ماهیچهها میشود با عدم توانایی راه رفتن ، ۹۶% معلولیت، انحنا در ستون فقرات و قفسه سینه، مشکلات تنفسی و مرگ خاتمه می یابد. سایر نشانهها و عوارض اصلی دوشن به شرح زیر است:
با آزمایش ژنتیک می توان به نوع جهش مسبب بیماری بر روی کزوموزوم X پی برد.
الکترومیوگرافی از بافت عضلانی نشان می دهد که تحلیل عضلات ناشی از با نفوذ شدن بافت عضلانی در اثر نقص در تولید پروتئین دیستروفین است نه در اثر اعصاب.
نمونه برداری از بافت ماهیچه ای و بررسی توسط روش IHC فقدان پروتئین دیستروفین را تایید می کند.
ژن دیستروفین مرکب از ۷۹ اگزون است و تجزیه و تحلیل تست DNA معمولاً نوع خاصی از جهش در اگزون یا اگزونهای فرد مبتلا را مشخص می کند. تست DNA در اکثر موارد ابتلای فرد به بیماری را تأیید می کند.
نزدیک به دو سوم از بیماران دارای یک حذف یا اضافه شدگی در ژن دیستروفین خود هستند و این دسته از بیماران را می توان به راحتی توسط تست های ژنتیکی شناسایی نمود ولی برای تأیید بیماری در یک سوم باقی مانده باید تمامی طول ين DMD را برای یافتن جهش های نقطه ای مورد بررسی قرار داد که تا حدی این روش زمان گیر و پر هزینه خواهد بود.
اگر تست DNA نتواند جهش در اگزونها را پیدا کند، ممکن است از ماهیچه نمونه برداری شود. نمونه کوچکی از ماهیچه استخراج شده (معمولاً با چاقوی کوچک جراحی به جای سوزن سرنگ) وضعیت فقدان کامل پروتئین دیستروفین را نشان می دهد. در طول چند سال گذشته تست DNA در زمینه شناسایی جهش هایی زیادی در ژنها که سبب ایجاد بیماریهای مختلف میشود پیشرفت داشته است و نمونه برداری از ماهیچه غالباً تنها بیماری دوشن را تأیید نمی کند.
اگر یکی یا هردو والدین حامل بیماری خاصی باشد، مبتلا شدن فرزند به دنیا نیامده آنها به آن بیماری ریسک است. آزمایش پیش از تولد برای پیدا کردن جنین مبتلا به دوشن در دوران بارداری انجام میشود، این آزمایشها تنها برای برخی از اختلالات عصبی و ماهیچه ای کاربرد دارد. انواع آزمایشهای پیش از تولد می تواند بعد از حدود ۱۱ هفته پس از بارداری به اجرا دربیاید. نمونه برداری از برآمدگی پرز های پرده بیرونی جنین (CVS) در هفته ۱۱ تا ۱۴ بارداری انجام و تست نمونه گیری از آمنیون مایع بعد از هفته ۱۵ بارداری انجام میشود، در حالی که نمونه خون جنین می تواند حدوداً در هفته ۱۸ بارداری صورت گیرد. زنان و یا زوجها باید دقت نظر داشته باشند که پس از انجام آزمایش در مورد آن با مشاور ژنتیک به بحث بنشیند. در صورتی که آزمایش پیش از تولد ابتلا جنین به بیماری دوشن را مشخص کند دستور سقط جنین صادر میشود تا از تولد نوزاد بیمار جلوگیری شود.
از آنجا که بیماری دوشن یک بیماری بسیار حاد است و در مدت کوتاهی زندگی بیماران و خانوادههای آنان را دگرگون میکند، عمدتاً مبتلایان به این بیماری را در کودکان، نوجوانان و جوانان تشکیل می دهند، به علت عدم پذیرش معلولیت از سوی مبتلایان و به خصوص جامعه ایران که برای بیماران هیچ گونه تعمهیدات، مناسب سازی و برنامه ای انجام نداده و عدم فرهنگ سازی که مردم با ترحم به بیماران نگاه می کنند.، موارد زیادی از افسردگی میان جوانان مبتلا به این بیماری وجود دارد. همچنین دیستروفی ماهیچه ای دوشن به دلیل نوع پیشرونده بودن بیماری، نهایتاً منجر به معلولیت شخص میشود، این موضوع می تواند عوارض روحی و روانی را در مبتلایان و خانوادههای آنها را به دنبال داشته باشد . به دلیل این مسأله حتی چند مورد خودکشی مادران بیماران گزارش شده است.
تاکنون هیچ درمانی برای دیستروفی ماهیچه ای دوشن یافت نشده است اگرچه اخیراً تحقیقات نشان می دهد به وسیله سلولهای بنیادی می توان بافت ماهیچههای سالم را جایگزین بافت ماهیچه ای آسیب دیده کرد. تنها با فیزیوتراپی و کاردرمانی می توان از انحراف ستون فقرات و قفسه سینه که موجب جمع شدگی بدن میشود جلوگیری کرد.
تحقیقات در حال اجرا
کارآزمایی بر روی "AVI ۴۶۵۸" که یک فرآورده آزمایشگاهی برای نادیده انگاشتن اگزونی در دیستروفی ماهیچه ای دوشن است موجب تولید دیستروفین شده و بی خطر به نظر می رسد. "AVI ۴۶۵۸" یک داروی آزمایشگاهی است که توسط شرکت "AVI BioPharma" برای نادیده انگاشتن اگزون ۵۱ ژن دیستروفین تولید شده است. نادیده انگاشتن اگزون ۵۱ توان بالقوه برای تولید پروتئین دیستروفین را در زیر مجموعه ای از افراد مبتلا به دیستروفی ماهیچه ای دوشن را دارد. هنگامی که دارو به شکل داخل وریدی داده شد، بی خطر به نظر رسید و سبب افزایش تولید دیستروفین در برخی از داوطلبین گردید. ۲۴ پسر بین ۵ تا ۱۵ سال دارای جهش دیستروفین در ناحیهٔ اگزون ۵۱ داروی "AVI ۴۶۵۸" را به شکل هفتگی به مدت ۱۲ هفته در یکی از شش مقیاس دوزاژ دریافت کردند. هر گروه نسبت به گروه قبلی مقدار بیشتری از دارو را دریافت کرد. دارو بی هیچ رویداد ناگواری تحمل گردید، هر چند در یکی از پسرها ضعف عضله قلبی ( کاردیو مایو پاتی ) تشدید شد و از کارآزمایی کنار گذاشته شد. اینکه آیا دارو سبب بروز این مشکل شد یا خیر مشخص نگردید، شرکت "AVI ۴۶۵۸" قصد ادامه آزمایش دارو را دارد.
محققان "بیمارستان اطفال پیتسبورگ" دسته منحصر به فردی از سلولهای بنیادی بزرگسال را شناسایی کردهاند که میتواند بیماریهایی نظیر حمله قلبی و دیستروفی ماهیچه ای دوشن را درمان کند. دانشمندان سلولهای بنیادی "میوآندوتلیال" myoendothelial را جداسازی و مشخص کردند، این سلولها با استفاده از فناوریهای جداسازی سلول به راحتی جدا میشوند، به سرعت تکثیر مییابند و میتوانند در محیط آزمایشگاه به سلولهای ماهیچه ای، استخوان و غضروف تمایز پیدا کنند. کشف این دسته سلولهای بنیادی در یک منبع انسانی موفقیت بزرگی به شمار میرود، زیرا به کاربرد بالینی این درمان بسیار نزدیکتر می شود. به گفته دانشمندان، پیوند هزار سلول میوآندوتلیال به ماهیچه آسیب دیده موشهایی که دچار نقص ایمنی بودند بطور متوسط ۸۹ لیف عضلانی تولید کرد.
اساس این بیماری کاملاً مشابه با بیماری دوشن می باشد و هر دوی آنها به دلیل بروز جهش در ژن DMD رخ می دهند. تنها تفاوت موجود بین این دو بیماری شدت آنها است به نحوی که برخی از جهش های ژن DMD در مقایسه با سایر جهش ها خفیف تر بوده و شدت علائمی که ایجاد می شود به مراتب خفیف تر هستند. در این گونه موارد گفته می شود که فرد به بیماری دیستروفی بکر مبتلا شده است. این گروه از بیماران در سنین بالاتری و در مواردی حتی بعد از بلوغ به بیماری مبتلا می شوند و بسیاری از آنان به معلولیت کامل دچار نمی شوند و تنها عضلات آنان ضعیف می شود ولی در بسیاری موارد این افراد به تنهایی قادر به اداره زندگی خود هستند.
دیستروفی های عضلانی دوشن و بکر همراه با هم 1 نفر در هر 3.500 تا 5.000 نوزاد مذکر تازه متولد شده در سراسر جهان را تحت تاثیر قرار میدهند. سالانه بین 400 تا 600 پسر در ایالات متحده آمریکا با این بیماری ها متولد میشوند.
این بیماری با الگوی توارث وابسته به X مغلوب به ارث میرسد. ژن مرتبط با این بیماری روی کروموزوم X که یکی از دو کروموزوم جنسی است قرار گرفته است. در افراد مذکر ( افرادی که تنها یک کروموزوم X دارند ) ، یک کپی تغییریافته از ژن در هر سلول برای ایجاد بیماری کافی است. در افراد مونث ( افرادی که دارای دو کروموزوم X میباشند ) ، یک جهش باید در دو کپی ژن ظاهر شود تا بیماری ایجاد شود. از آنجائیکه احتمال اینکه افراد مونث دو کپی تغییریافته از این ژن داشته باشند وجود ندارد ، افراد مذکر مبتلا به اختلالات وابسته به X مغلوب نسبت به افراد مونث بسیار فراوان تر میباشند. ویژگی بارز توارث وابسته به X این است که پدران نمیتوانند صفات وابسته به X را به پسران خود انتقال دهند. در بسیاری موارد ، فرد مذکر مبتلا جهش را از مادر خود که یک کپی تغییریافته از ژن DMD را حمل میکند به ارث میبرد. باقی موارد احتمالا از جهش های جدید در ژن مذکران مبتلا نشات میگیرند و ارثی نیستند. در توارث وابسته به X مغلوب ، یک فرد مونث با یک کپی جهش یافته از ژن در هر سلول ، حامل نامیده میشود. او میتواند ژن تغییریافته را انتقال دهد اما معمولا علائم بیماری را تجربه نمیکند. گرچه ، گاهی افراد مونث حامل یک جهش در ژن DMD ممکن است دارای ضعف و گرفتگی عضلانی باشند. این علائم معمولا نسبت به ضعف و تحلیل عضلانی شدید مشاهده شده در مذکران مبتلا ملایم تر است. افراد مونث حامل جهش ژنی DMD دارای افزایش ریسک کسب اختلالات قلبی از جمله کاردیومیوپاتی نیز میباشند.